La CNS tient à disposition du laboratoire le fichier électronique correspondant à la description du layout du fichier autorisation (.xsd). Les zones et données obligatoires sont décrites au cahier des charges à l'annexe X. Les formatages et structures publiées sur le site de la CNS sont à utiliser impérativement. Toute évolution technique du layout est signalée au laboratoire qui dispose d'un délai de 3 mois pour s'y conformer.
Dans le cadre d’une matérialisation de la demande d’autorisation, elle doit être établie conformément au modèle prévu à l’annexe IX du cahier des charges. Ce document est publié sur le site de la CNS.
Gestion des demandes d'autorisation
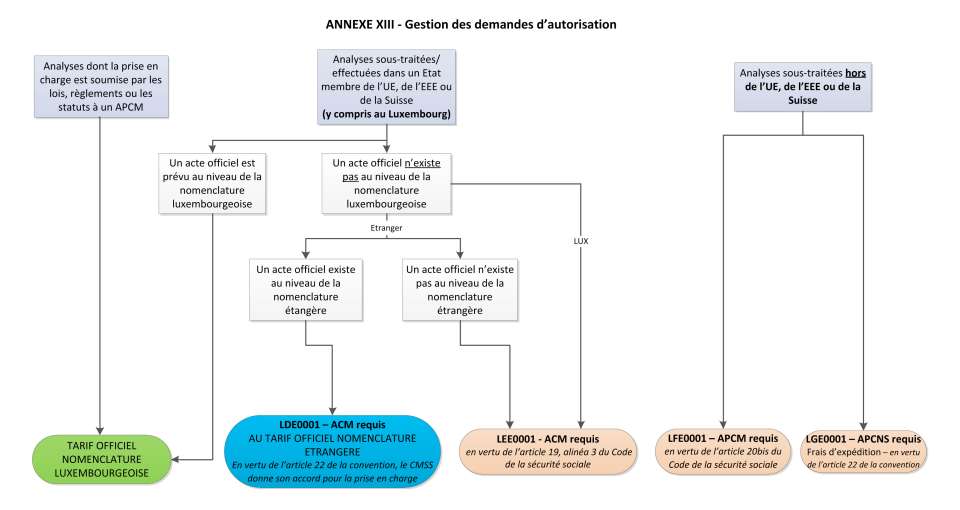
Conformément aux dispositions de l'article 23 du cahier des charges relatif aux documents et formules standardisés conclue entre la Fédération luxembourgeoise des Laboratoires d'analyses médicales et la Caisse nationale de santé, les codes collectifs suivants sont utilisés en fonction de la procédure de demande d'autorisation appliquée :
LDE0001 - ACM requis
Analyse sous-traitée/effectuée dans un Etat membre de l'UE, de l'EEE ou de la Suisse, pour laquelle aucun acte officiel n'existe au niveau de la nomenclature luxembourgeoise des actes de laboratoires d’analyses médicales mais pour laquelle un acte officiel figure dans la nomenclature des analyses prises en charge dans le cadre de l’assurance maladie légale dans le pays (UE, EEE ou Suisse) où elle est effectuée. Dans ce cas la procédure en vertu de l’article 22 de la convention est appliquée. L'alinéa 2 énonce:
Lorsque l’analyse a été transmise et effectuée dans un laboratoire situé en dehors du Grand-Duché de Luxembourg, mais dans un pays de l’UE, de l’EEE ou en Suisse et qu’un tarif y relatif n’est pas prévu par la nomenclature des actes et services des laboratoires d’analyses médicales et de biologie clinique au Luxembourg, elle est facturée par le laboratoire transmetteur conformément au tarif officiel opposable à l’assurance maladie légale dans l’Etat dans lequel l’analyse a été effectuée, à condition qu’elle tombe dans le champ d’application matériel de l’assurance maladie au Luxembourg, et que le Contrôle médical de la sécurité sociale ait donné son accord pour la prise en charge.
LEE0001 - ACM requis
Analyse exceptionnelle ne figurant ni dans la nomenclature luxembourgeoise des actes de laboratoires d’analyses médicales ni dans celle des analyses prises en charge dans le cadre de l’assurance maladie légale dans le pays (UE, EEE ou Suisse) où elle est effectuée. La procédure en vertu de l’article 19, alinéa 3 du Code de la sécurité sociale est appliquée.
LFE0001 - APCM requis
Analyse exceptionnelle, sous traitée hors de l'UE, de l'EEE ou de la Suisse, ne figurant pas dans la nomenclature des actes de laboratoires d’analyses médicales. - La procédure en vertu de article 20bis du Code de la sécurité sociale est appliquée.
En conformité avec l'article 19, alinéa 3 et l'article 20bis du Code la sécurité sociale, l'article 22 alinéa 3 de la convention entre la Fédération luxembourgeoise des Laboratoires d’analyses médicales et la Caisse nationale de santé énonce:
A défaut d’un tarif officiel opposable à l’assurance maladie légale dans l’Etat membre dans lequel le laboratoire de collaboration est établi, mais que l’analyse tombe dans le champ d’application matériel de l’assurance maladie au Luxembourg, sans pour autant figurer dans la nomenclature des actes et services des laboratoires d’analyses médicales et de biologie clinique au Luxembourg, le remboursement par l’assurance maladie se fait sur base d’un tarif fixé par le Contrôle médical de la sécurité sociale assimilant la prestation exceptionnelle à une prestation de même importance. Il en est de même pour les analyses effectuées conformément aux conditions et modalités de la présente convention en dehors d’un pays de l’UE, de l’EEE ou de la Suisse.
LGE0001 - APCNS requis
Frais d’expédition en cas de transfert d’analyse hors de l’UE, de l’EEE ou de la Suisse. - La procédure en vertu de l’article 22 de la convention est appliquée. L'alinéa 5 énonce:
Dans les cas exceptionnels pour des analyses ne figurant pas dans la nomenclature des actes et services des laboratoires d’analyses de biologie médicale et ne pouvant pas être effectuées au Luxembourg ou dans un pays de l’UE, de l’EEE ou en Suisse, il est tenu compte des frais d’expédition exposés par le laboratoire transmetteur pour le transfert des prélèvements. La prise en charge des frais d’expédition est subordonnée à une autorisation préalable de la Caisse nationale de santé pour la transmission des analyses dans un pays en dehors de l’UE, de l’EEE et de la Suisse conformément à l’article 9 de la présente convention et à une justification des frais d’expédition par le laboratoire transmetteur.
Chaque analyse fait l’objet d’une demande séparée.
Les demandes de prise en charge des frais d’expédition hors de l’UE, de l’EEE ou de la Suisse sont formulées sur la même demande que l’analyse s’y rapportant. Les frais d’expédition sont documentés par un devis émis par le transporteur. La prise en charge des frais d’expédition est conditionnée par la prise en charge des analyses s’y rapportant.

